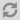Medizin: Diese Nanostrukturen „erstechen“ Bakterien mit winzigen Metallspitzen
Bakterien gehören zu den hartnäckigsten Untermietern, die sich auf Oberflächen aller Art festsetzen können. Ob auf Implantaten, in Rohrleitungen oder auf Schiffsrümpfen: Sobald sich die winzigen Organismen erst einmal angesiedelt haben, bauen sie eine widerstandsfähige Schleimschicht auf, die sie nahezu unverwundbar macht. Biofilme sind deshalb nicht nur lästig, sondern verursachen weltweit medizinische Komplikationen, industrielle Ausfälle und erhebliche Kosten. Obwohl seit Jahren an Strategien gegen diese problematischen Besiedlungen geforscht wird, dominieren weiterhin chemische Methoden den Alltag – darunter Antibiotika oder Metallionen. Die damit verbundenen Risiken wie Resistenzbildung oder Umweltbelastungen sind jedoch nur schwer zu ignorieren.
Genau hier setzt eine andere Herangehensweise an, die nicht auf chemische Kampfstoffe setzt, sondern auf reine Mechanik. Forschende in Schweden und Deutschland haben gezeigt, dass bestimmte Metal–Organic Frameworks (MOFs) zu Oberflächen geformt werden können, die Bakterien beim Kontakt physisch zerstören. Diese Materialien, bekannt geworden als Speichermedien für Gase oder als vielseitige Filterstrukturen, erhalten damit ein neues Wirkprinzip, das das Entstehen von Biofilmen schon beim ersten Kontakt verhindert. Eine Forscherin beschreibt das Funktionsprinzip als „eine nanoskalige Landschaft aus Spitzen, die jede Zelle trifft, bevor sie sich überhaupt orientieren kann“.
Strukturierte MOFs gegen die Bildung von Biofilmen
Biofilme entstehen, wenn Bakterien sich an einer Oberfläche festsetzen und eine schützende Matrix aufbauen. Diese Matrix macht sie besonders widerstandsfähig gegenüber äußeren Einflüssen und erschwert sowohl Reinigung als auch medizinische Behandlung. In Krankenhäusern tragen solche Besiedlungen zu Infektionen rund um Implantate und Katheter bei, während sie in industriellen Anlagen Korrosion fördern oder Strömungswege blockieren können. Konventionelle antibakterielle Beschichtungen versuchen daher meist, Mikroben chemisch zu schwächen oder abzutöten. Doch die ständige Exposition gegenüber solchen Stoffen erhöht langfristig das Risiko resistenter Stämme.
Die neuen MOF-basierten Oberflächen verfolgen einen anderen Ansatz: Sie arbeiten völlig ohne Chemikalien. Bei der Herstellung bilden sich nanometergroße Spitzen aus, die so ausgerichtet sind, dass sie die Zellmembran der Bakterien beim Kontakt durchstoßen. Entscheidend dabei ist der korrekte Abstand dieser Spitzen. Sind sie zu eng gesetzt, verteilt sich die Belastung zu stark, was den mechanischen Effekt aufhebt. Sind sie zu weit auseinander, finden die Mikroben Zwischenräume, in denen sie sich niederlassen können. Die präzise Kontrolle der Kristallisationsbedingungen war daher ein zentraler Schritt, um funktionale, reproduzierbare Strukturen zu erzeugen. Ein beteiligter Forscher formuliert es so: „Es ist wie ein Nagelbrett im Nanomaßstab – nur mit genau der richtigen Anordnung, damit kein Bakterium ungeschoren davonkommt.“
Neuer Ansatz erzeugt keine Resistenzen
Der mechanische Wirkmechanismus hat mehrere Vorteile. Da keine antibiotischen Substanzen eingesetzt werden, entsteht kein Selektionsdruck, der resistente Bakterienstämme begünstigt. Auch die Umwelt wird geschont, weil keine toxischen Metalle oder Biozide freigesetzt werden. Die MOF-Beschichtungen können außerdem bei relativ niedrigen Temperaturen hergestellt werden, wodurch sich auch empfindliche Materialien beschichten lassen, wie sie etwa in medizinischen Geräten oder flexiblem Kunststoff vorkommen.
Darüber hinaus eröffnet die Struktur der MOFs die Möglichkeit, die organischen Bausteine aus recycelten Kunststoffen zu gewinnen, was den ökologischen Fußabdruck weiter reduziert. Denkbar sind Anwendungen in zahlreichen Bereichen: Implantate und Katheter könnten länger keimfrei bleiben, industrielle Anlagen weniger häufig gewartet werden müssen, und schiffsnahe Oberflächen ließen sich vor mikrobieller Besiedlung schützen, ohne auf schädliche Anti-Fouling-Beschichtungen zurückzugreifen.
Die Ergebnisse zeigen, dass MOFs weit mehr können als Speicher- oder Filteraufgaben übernehmen. Sie lassen sich als aktive, verteidigende Oberflächen gestalten, die Bakterien allein durch ihre Struktur zuverlässig fernhalten. Damit entsteht eine neue Klasse antibakterieller Materialien, die auf Nachhaltigkeit, physikalische Wirksamkeit und auf ein minimiertes Risiko von Resistenzen setzt. Die Arbeiten bieten einen deutlichen Hinweis darauf, dass die Zukunft der antibakteriellen Technologie nicht nur im chemischen Labor liegt, sondern genauso im präzise konstruierten Mikro- und Nanodesign von Materialien.